식약처, 2021년 의약품 품목갱신 결과 공개
2022.02.17 식품의약품안전처
|
식약처, 2021년 의약품 품목갱신 결과 공개
- 품목갱신 통해 4,165품목 정리, 1,009품목 허가변경 등 안전조치-
|
□ 식품의약품안전처(처장 김강립)는 허가·신고된 의약품을 주기적이고 체계적으로 관리하기 위해 시행되고 있는 ‘의약품 품목갱신 제도’의 2021년 의약품 품목갱신 결과를 공개했습니다.
○ 의약품 품목갱신 제도는 2018년부터 본격 시행됐으며 이미 허가·신고된 의약품을 5년 주기(1주기: ’18∼’23)로 ▲안전성·유효성 등 안전관리자료 ▲품질관리자료 ▲표시기재자료 ▲제조·수입실적 등을 평가하는 제도입니다.
- 이번 2021년 의약품 품목갱신 결과에는 2018년 제도 시행 이후 지난 4년(’18~’21년)간의 의약품 품목갱신 결과도 함께 담았습니다.
□ 식약처는 지난 4년간 품목갱신 검토 결과를 바탕으로 의약품의 안전한 사용 강화를 위한 허가사항 변경 명령과 안전성·유효성 재확인을 위한 임상 재평가 공고 등 안전조치를 실시한 바 있습니다.
○ 지난 4년간 ‘아스피린제제(진통제)’ 등 105개 성분(2,265개 품목)의 효능·효과, 용법·용량 개선 등 허가·신고사항 변경을 명령했고, ‘포르모테롤푸마르산염제제(기관지천식약)’ 등 총 9개 성분(66개 품목)에 대해서는 안전성·유효성의 재입증을 위한 임상재평가 실시를 공고했습니다.
○ 특히 2021년에는 총 38개 성분(1,009개 품목)에 대해 허가·신고사항 변경을 명령했으며, 처음 3년간(’18∼‘20)의 총 67개 성분(1,256개 품목) 대비 큰 폭으로 증가한 수치입니다.
- 이는 의약품 품목갱신 제도 본격 운영 4년 차를 지나며 허가·신고된 의약품의 주기적·체계적 관리 수준이 향상되는 등 의약품 품목갱신 제도가 일정 수준 정착 단계에 도달한 결과로 분석됩니다.
□ 식약처는 의약품 품목갱신 1주기(’18∼’23) 대상 총 4만 6,064개 품목 중 4년(’18∼’21)동안 63%(2만 8,857개 품목, 누적)를 진행했습니다.
* 연도별 갱신 대상 품목 현황(전체 대비 누적 %): (’18년) 4,798개(10%) → (’19년) 7,571개(27%) → (’20년) 8,083개(44%) → (’21년) 8,405개 63% → (’22년) 7,303개(78%) → (’23년 6월) 9,904개(100%)
○ 2021년까지 지난 4년간 품목갱신이 진행된 2만8,857개 품목 중 1만7,461개 품목(61%)의 갱신이 완료됐으나, 1만 1,396개 품목(39%)은 유효기간 만료 등*으로 정리됐습니다.
* 수출 전용 품목으로 전환, 업체에서의 품목 취하 포함
- 2021년의 경우, 품목갱신 대상 8,405개 품목 중 4,240개(50%)품목은 갱신됐고, 4,165개(50%) 품목은 유효기간 만료 등으로 정리됐습니다.
□ 식약처는 품목갱신 결과 공개가 업계의 의약품 품목갱신 제도에 대한 이해도를 향상시키고 제품 개발·출시를 위한 허가·신고 품목 현황을 파악하는 데 도움을 줄 수 있을 것으로 기대합니다.
○ 앞으로도 규제 전문성과 과학적 지식을 바탕으로 의약품 품목갱신 제도를 안정적으로 정착시키고 의약품의 주기적·체계적 품목허가 관리 수준을 높일 수 있도록 적극 노력하겠습니다.
* 이번 ‘2021년도 의약품 품목갱신 보고서’는 식약처 대표 누리집 (mfds.go.kr) → 법령/자료 → 자료실 → 매뉴얼/지침에서 확인할 수 있음
<붙임> 1. 의약품 품목갱신 제도 개요
2. 의약품 품목갱신 현황
|
붙임 1
|
|
의약품 품목 갱신제도 개요
|
□ 제도 개요
❍ (목적) 의약품의 품목허가․신고 이후 안전성․유효성을 지속 확보하고 품목의 효율적인 관리를 위해 5년마다 품목허가․신고를 갱신
※ 근거 법령 :「약사법」제31조의5 (‘12.5.14 개정, ʹ13.1.1. 시행),「의약품 등의 안전에 관한 규칙」제20조 (‘12.10 개정), 의약품 품목 갱신에 관한 규정(고시) (‘16.9 제정)
❍ (적용대상) 「약사법」제31조제2항, 제3항 및 제42조에 따른 품목허가․신고된 모든 의약품. 다만, 원료의약품과 수출용의약품은 제외
❍ (유효기간) ’13년 이후 허가 품목은 허가․신고 시에 5년, ’13년 이전 허가된 품목은 분류번호 별로 ’18.9.30.~’23.6.30. 중 만료일을 부여
❍ (제출자료) 품목별로 유효기간 동안 해당 업체가 관리 운영한 안전관리·품질·제조실적 등에 관한 자료를 제출
* ①부작용보고 등 안전관리 자료 ②외국 사용현황 자료 ③품질관리 자료 ④표시기재 자료 ⑤제조·수입실적 ⑥허가증
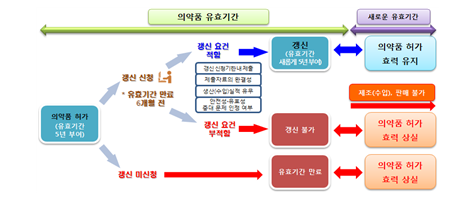
❍ (갱신 절차)
- 유효기간 만료 6개월 전까지 해당 품목허가․신고 발급기관(본부, 지방청)에 갱신 신청
- 제출자료는 유효기간 동안 품목의 안전성․유효성, 품질, 생산실적 등 관련 정보를 확인할 수 있는 증명자료나 사유서 등
|
붙임 2
|
|
의약품 품목갱신 현황
|
□ 연도별 갱신 현황
(단위: 품목수, ’21.12월 기준)
|
구분
|
계
(’18~’21)
|
’18년
|
’19년
|
’20년
|
’21년
|
’22년
|
’23년~
|
|
갱신 대상
|
28,857개
|
4,798개
|
7,571개
|
8,083개
|
8,405개
|
7,303개
|
9,904개
|
|
갱신 완료
(대상대비, %)
|
17,461개
(61%)
|
3,128개
(65%)
|
5,144개
(68%)
|
4,949개
(61%)
|
4,240개
(50%)
|
|
|
□ 2021년 갱신 결과
(단위: 품목수, ’21.12월 기준)
|
구분
|
갱신 대상
|
갱신 완료
|
미갱신
|
|
|
총 계
|
8,405개
|
4,240개 (50%)
|
4,165개 (50%)
|
|
|
제조
‧
수입
|
제조 품목
|
7,776개
|
3,866개 (50%)
|
3,910개 (50%)
|
|
수입 품목
|
629개
|
374개 (59%)
|
255개 (41%)
|
|
|
전문
‧
일반
|
전문의약품
|
4,090개
|
2,626개 (64%)
|
1,464개 (36%)
|
|
일반의약품
|
4,315개
|
1,614개 (37%)
|
2,701개 (63%)
|
|
□ 2021년 갱신 완료 현황
(단위: 품목수, ’21.12월 기준)
|
총 계
|
4,240개
|
화학의약품
|
생물의약품
|
한약(생약)제제
|
|
|
3,831개
(90.4%)
|
94개
(2.2%)
|
315개
(7.4%)
|
|||
|
제조
‧
수입
|
제조
|
3,866개
(91%)
|
3,525개
(92%)
|
45개
(48%)
|
296개
(94%)
|
|
수입
|
374개
(9%)
|
306개
(8%)
|
49개
(52%)
|
19개
(6%)
|
|
|
허가
‧
신고
|
허가
|
1,698개
(40%)
|
1,560개
(41%)
|
94개
(100%)
|
44개
(14%)
|
|
신고
|
2,542개
(60%)
|
2,271개
(59%)
|
0개
(0%)
|
271개
(86%)
|
|
|
전문
‧
일반
|
전문
|
2,626개
(62%)
|
2,489개
(81%)
|
94개
(100%)
|
43개
(14%)
|
|
일반
|
1,614개
(38%)
|
1,342개
(19%)
|
0개
(0%)
|
272개
(86%)
|
|
'알면 도움이 되는 정책 및 지원사업 > 정부 정책뉴스' 카테고리의 다른 글
| 하도급분야 비밀유지 계약체결 의무화_공정거래위원회 (0) | 2022.02.17 |
|---|---|
| 통계지리정보서비스(SGIS), 도시화 분석 지도, 행정통계 시각화 지도 등 서비스 개시_통계청 (0) | 2022.02.17 |
| 노란달걀버섯에서 헬리코박터균 억제 물질 발견_산림청 (1) | 2022.02.17 |
| 온라인동영상서비스 콘텐츠 분야 석사급 전문 인재 기른다_문화체육관광부 (1) | 2022.02.17 |
| 2022년도 과기정통부 디지털 뉴딜 사업 설명회 개최_과학기술정보통신부 (0) | 2022.02.16 |


댓글